1 主题内容与适用范围
本标准规定了以活性炭为主要吸附剂,以去除有机物为目的的饮水净器(以下简称净水器)的技术要求,试验方法和检验规则。
本标准适用于以自来水为进水的供家庭和集团饮用的活性炭净水器。
2 引用标准
GB 5749 生活饮用水卫生标准
GB 5750 生活饮用水标准检验法
GB 8538 饮用天然矿泉水检验方法
GB 4804 搪瓷食具容器卫生标准
搪瓷食具卫生管理办法
GB 2633 日用搪瓷制品检验方法
GB 4803 食品包装用聚氯乙烯树脂卫生标准
食品用塑料制品及原材料卫生管理办法
GB 7702 煤质颗粒活性炭—有效防护时间测定总方法
GB 601 标准溶液制备方法
GBn 84 聚乙烯成型品卫生标准
GBn 85 聚丙烯成型品卫生标准
GBn 86 聚苯乙烯成型品卫生标准
GB 9684 不锈钢食具容器卫生标准
GB 4807 食用橡胶垫片(圈)卫生标准
GB 4805 食品罐头内壁环氧酚醛涂料卫生标准
QJ 1289 结构钢、不锈钢电阻点,缝焊技术条件
3 术语
3.1 集团用 For drinking purpose of groups or ouganizations
指供学校、厂矿、机关、宾馆等团体使用。
3.2 产水率 Rate of out flow
每分钟经净水器产出的水量,以L/min计。
3.3 额定总产水量 Rated total output capacity
净水器中活性炭的吸附容量所能承受的产水量总和,L(家庭用)或m3(集团用)。
3.4 相对产水率 Relative rate of out flow
以活性炭体积倍数计算的净水器每分钟的产水量即空间流速以min-1计。
3.5 相对总产水量 Relative total output capacity
以活性炭体积的倍数计算的净水器累计产水总量。
4 产品分类
4.1 产品品种
家庭用净水器和集团用净水器。
4.2 产品型号与标记
产品标记由产品名称,品种代号,质量等级代号,产水率代号和额定总产水量代号组成。
××× ×× ×× × ×
其中:×××——活性炭净水器;
××——家庭用或集团用;
××——质量等级;
×——产水率;
×——额定总产水量。
4.2.1 家庭用净水器的代号为H,集团净水器代号为G。
4.2.2 质量等级的代表为A或B。A表示一级品,B表示二级品。
[例1]家庭用活性炭净水器,装活性炭1L,一级品,产水率1.0Lmin,额定总产水量2000L,产品型号及标记为:
活性炭净水器 HA 1.0 200
[例2]集团用活性炭净水器,装活性炭体积0.2m3,二级品,出水率10L/min,额定总产水量200m3。产品型号及标记为:
活性炭净水器 GB 10 200
5 技术要求
5.1 材料要求
5.1.1 与水接触的净水器壳体和管道采用的搪瓷、塑料或不锈钢材料应分别符合GB4804、GB4803、GB9684、GBn9684、GBn85、GBn86的规定。
5.1.2 用以截留悬浮物的纤维网布或多孔滤膜,滤片和滤柱应是食品级材料制成。或经当地卫生监督部门检验核准的材料。
5.1.3 净水器所用橡胶垫片(圈)的卫生要求应符合国际GB4807的规定。
5.1.4 净水器内壁涂料应符合GB4805的规定。
5.1.5 净水器采用的颗粒活性炭应符合表1的要求:
表1 颗粒活性炭技术要求
| 项 目 | 指 标 | | A级净水器用 | B级净水器用 | | 水 份(%) | ≤5 | ≤5 | | 强 度(%)(球磨法) | ≥90 | ≥85 | | 碘吸附值(mg/g) | ≥1000 | ≥800 | | 亚甲兰吸附值(mg/g) | ≥135 | ≥105 | | 苯酚吸附值(mg/g) | ≥120 | ≥120 | | 半脱氯值(cm) | ≤6.0 | ≤8.0 | | 堆集密度(g/cm3) | ≤0.5 | ≤0.5 | | 粒 度 | 不规定 | | pH | 4~11 | | 氯化物 (%) | ≤0.5 | | 铅 (µg/g) | ≤10 | | 锌 (µg/g) | ≤50 | | 镉 (µg/g) | ≤1 | | 砷 (µg/g) | ≤2 | 5.2 制作要求
5.2.1 净水器活性炭过滤柱的有效高度与直径之比采用2~6为宜。
5.2.2 管道、管件要求应横平、竖直,法兰要求应上下平行。
5.2.3 过水容器应在规定试验压力下无渗漏、损坏。
5.2.4 搪瓷筒体应按GB2633方法检验,其密着性能试验不得呈块状;耐热骤变试验不得掉瓷;耐碱试验不得失去原有的光泽;耐酸试验侵蚀≤0.2mg/mL。
5.2.5 塑料筒体对称部位壁厚比不应大于3:2,嘴口要求应平整,废边应整修光滑,螺纹清晰,配合适宜。
5.2.6 不锈钢筒体的焊接应符合QJ1289的要求。
5.3 装配要求
5.3.1 与水接触的所有零部件必须经清洗和消毒。
5.3.2 活性炭在放入容器前应先装入尼龙筛绢网,并进行清洗消毒和干燥处理。
5.3.3 净水器各零部件的装配应保证无松动现象发生,并便于更换活性炭。
5.4 外观要求
5.4.1 搪瓷筒体外表应符合GB4804的要求。
5.4.2 塑料筒体外表不应有砂眼或塑化不良,应光滑平整,不应夹带杂质或表面凹凸等明显有损外观的缺陷。
5.4.3 不锈钢筒体外表应光亮,不应有明显影响外观的缺陷。
5.4.4 筒体外表应有明显的产品标志。
5.5 净水器的消毒设备要求
5.5.1 净水器是否带消毒设备应在产品说明书中予以说明。供生饮用的净水器必须带消毒设备。
5.5.2 净水器的消毒可采用紫外灯,次氯酸钠发生器,臭氧发生器,超滤膜过滤器或其他合适的消毒设备或措施。
5.5.3 消毒设备与措施应与净水器的产水率及额定总产水量相适应,以保证净水器出水水质符合GB5749中细菌学的要求。
5.6 使用性能要求
5.6.1 集团用净水器及其附属设备应保证在0.2MPa工作压力下无泄漏,筒体不变形。家用净水器应在0.1MPa工作压力下无泄漏,筒体不变形。
5.6.2 净水器及其附属设备的产水率应保证在0.2MPa工作压力下,不应小于标记产水率。净水器的产水率及额定总产水量应根据活性炭的吸附容量确定。
5.6.3 净水器在标记额定总产水量到达前,其出水水质应优于GB5749的要求,亚硝酸盐氮应小于0.03mg/L。
5.6.4 当净水器进水水质中个别有机物指标超过生活饮用水卫生标准限值时,净水器对该指标在相对总产水量到达前应有一定的去除率。
5.6.5 采用三碘树脂消毒的净水器出水中含碘化物的浓度不得超过0.05mg/L。
5.6.6 进水耗氧量(高锰酸钾指数)CODMn 为4.0mg/L,溶解性有机碳DOC为6.0mg/L时,在相对产水率的条件下运行的净水器的净水效率应符合表2要求。
6 试验方法
6.1 生产厂应按5.1.1~5.1.5所列要求,提出有关的检验合格证书。
6.2 活性炭的质量应按GB7702规定的测定方法进行测定。
半脱氯值、pH、氯化物、砷、锌、镉、铅的测定方法见附录A,附录B 。
6.3 5.2要求应按有关规定进行。
6.4 5.3~5.5要求按生产厂检验规范进行检查。
6.5 应采用1.5级压力表在封闭出水口的条件下进行净水器的压力试验。
6.6 净水器产水率在进水压力为0.2MPa时,应用转子流量计测定,或用秒表量筒测定。
表2 活性炭净水器净水效率 | 项 目 | 指 标 | A级产品相对产
水率(min-1) | B级产品相对产
水率(min-1) | | 1.0 | 0.2 | 1.0 | 0.2 | | 1.相对总产水量 | ≥1200 | ≥2400 | ≥600 | ≥1200 | 2.额定相对总产水量到达前出水
耗氧量CODMn瞬时去除率(%)
总溶解性有机碳DOC瞬时去除率(%) | ≥25
≥25 | ≥15
≥15 | 3.额定相对总产水量到达前
CODMn总去除量(g/L炭)
DOC总去除量(g/L炭) | ≥2.5 ≥5.0
≥4.0 ≥8.0 | ≥1.0 ≥2.0
≥1.5 ≥3.0 | 4.额定相对总产水量到达前出水的Ames致突变试验
(1)进水为阳性时
(2)进水为阴性时 | 阴 性
阴 性 | 阴 性
阴 性 | 注:当进水的CODMn。DOC与上述指标不同时,应按进水的CODMn和DOC实际值折算相对总产水率。
6.7 家用净水器应在相对产水率为1.0min-1时检验出水质;集团用净水器应在相对产水率为0.2min-1时检验出水水质。产品的标记产水率与规定的相对产水率不一致时,应按大的产水率进行检验出水水质。
6.8 为检验净水器的净水效率,净水率应按6.7规定的产水率,至少每天采进出水水样测定CODMn及DOC或其他水质指标(视需要而定),直至总产水量超过相对产水率为止:或将采集的水样等量混和后,测定混和水样的CODMn及DOC或其他指标,并按表2中第1、第3项指标考核,但最后一次采集的水样需单独采集,并按表2的第2、第4项指标考核。
6.9 净水器出水水质应按GB5750的检验法检验,磺化物检验应按GB8538分析方法检验。总溶解性有机碳DOC及Ames致突变的试验方法见附录C、附录D。
7 检验规则
7.1 净水器的产品检验分为出厂检验和型式检验。
7.2 出厂检验
7.2.1 净水器在出厂前必须按规定的项目及试验方法进行出厂检验,合格后方可出厂。
7.2.2 出厂检验项目
出厂检验项目包括本标准5.1~5.5的各项规定,用目视法解体检查。
7.2.3 经出厂检验的产品数,家用净水器应不少于出厂净水器产品数的1/100;集团用净水器应不少于出厂净水器数的1/10。
7.3 型式检验
7.3.1 有下列情况之一时,应进行型式检验
a.新产品或老产品转厂生产的试制定型鉴定;
b.正式生产后,如结构、材料、工艺有较大改变,可能影响产品性能时;
c.正常生产后,定期或积累一定产量后,(由当地技术监督部门规定)应周期性进行一次检验;
d.产品长期停产后,恢复生产时;
e.出厂检验结果与上次型式试验有较大差异时;
f.国家质量监督机构提出进行型式检验要求时。
7.3.2 型式检验应按本标准第5章中各项技术要求和第6章规定的试验方法进行。
7.3.3 型式检验应直接从市场随机采样,每一型号的产品,应采取2只试样;一只按5.1~5.5的规定检验,一只按5.6的规定检验。
7.3.4 型式检验不合格的产品,应限期生产厂进行改进,到期复验。
8 判定规则
8.1 经检验凡属于下列情况之一者为不合格产品;
8.1.1 制作净水器的材料不符合5.1的要求者为不合格产品。
8.1.2 净水器的制作、装配,外观不符合5.2、5.3及5.4的要求者为不合格产品。
8.1.3 水压力试验不合格的产品为不合格产品。
8.1.4 净水器在相对总产水量到达前发生下列情况之一者即为不合格产品:
a.包括GB5749感官性状和一般化学指标中的色度,浑浊度,挥发酚,阳离子合成洗涤剂4项指标;毒理学指标所含15个指标;放射性指标中所含2个指标,亚硝酸盐氮;以及采用三碘树脂时出水中的碘化物;本标准表2所列净水效率1~3项指标在内的一共26项指标中A级产品同时发生2项不符合各自标准的要求,B级产品同时发生4项不符合各自标准的要求;
b.带有消毒装置或措施的供生饮的净水器,细菌总数或总大肠菌群有一项不符合GB5749的要求;
c.Ames致突变试验不符合本标准表2的要求。
9 标志、包装、运输和贮存
9.1 每只净水器应在规定的位置上固定铭牌,铭牌的内容规定如下:
a.制造厂名及商标;
b.产品名称及型号标记;
c.产品制造编号(或日期)或生产批号;
d.产品的主要参数—活性炭体积、产水率、额定产水率、额定总产水量;
e.工作压力;
f.质量等级标志;
g.有无消毒装置。
9.2 包装
9.2.1 包装方法:家用净水器用硬纸箱包装;集团用净水器视其重量决定用硬纸箱包装或木箱包装。
9.2.2 包装应防潮、防震、净水器进水和出水口应有防护套,包装件外形尺寸应符合国内外运输方法的有关规定,包装顶部宜为平顶。
9.2.3 产品装箱前应使其重心位置居中靠下,重心偏高的产品应尽可能采用卧式包装,重心偏离中心较明显的产品应采取相应的平衡措施。
9.2.4 包装箱应有足够的强度,起吊试验,堆垛试验和公路运输试验,应符合有关的规定。
9.2.5 产品应进行防雨包装,在箱内采取必要的防雨措施,可在产品外部罩塑料罩,包装箱顶盖应采用双层防水材料。
9.2.6 包装标志应使用冲洗不掉的油漆、油墨等准确、清晰、牢固地喷刷或印刷在箱面上,其标志包括:
a.产品型号、名称、规格和数量;
b.箱号;
c.箱体最大外形尺寸L×b×h(mm);
d.净重与毛重(kg);
e.中华人民共和国制造(国内发运不需如此标志)。
9.2.7 产品分多箱包装时,箱号应采用分数表示,分子为箱号、分母为总箱数,主件箱应为1号箱。
9.2.8 凡需起吊的和重心明显偏离中心的包装件,应标注“由此起吊”和“重心”的标志,并准确喷刷在包装件相应的位置上。
9.2.9 随带文件
a.使用说明书
说明使用方法,注意事项,装入的活性炭体积,亚硝酸盐氮控制(大于0.03mg/L时应清洗活性炭,活性炭清洗或更换条件及更换方法),不带消毒装置的净水器必须说明出水不能生饮;
b.产品合格证;
c.装箱单;
d.备附件清单;
e.其他有关技术资料。
分离包装时,随带文件应放在主件箱内。
附录A 净水器用活性炭半脱氯值测定方法(补充件)
A1 原理
在给定条件下,含氯水通过活性炭层后,出水中余氯浓度恰好等于进水中余氯浓度1/2时所需要的炭层高度,被称为活性炭的半脱氯值,以“cm”表示。
设在给定的流速下,余氯浓度为C0的水通过高度为L的炭层后,出水浓度为C,则有:
1og=C0/C=KL (A1)
式中 系数K与水的流速u有关。而实验表明,u与L有如下关系:
 (A2) (A2)
式中 h为半脱氯值。
为求K值,由A1、A2式得:
K=1ogC0/C/hu (A3)
根据半脱氯值定义,令C=1/2C0,且令u=1cm/s
则有:
K=log2/1/h=0.301/h (A4)
代入A1式得
logC0/C= 0.301/h L (A5)
即: h=0.301L /logC0-logC (A6)
通过(A6)式,即可在水流速度为1cm/s的条件下,从已知装炭高度L和进出水浓度C0及C,计算出半脱氯值h。
A2 仪器和试剂
A2.1 仪器
a.水槽 501。
b.测定管 截面积3.14±0.26cm2,结构及尺寸见GB 7702《煤炭颗粒活性炭—有效防护时间测定总方法》附录A《防护时间测定管及其校正方法》。
c.转子流量计 LZB-6型,2.5~25L/n。
d.振荡器 振幅≤2mm,频率10~25Hz。
e.pH酸度计
f..温度计 100°C
g.试验筛 筛孔1.0和2.5mm
h.秒表
i.微量滴定管 5mL
j.容量瓶 200mL和500mL
k.研钵
l.烧杯 250mL
m.三角瓶 500mL和1000mL
A2.2 试剂
a.碘化钾(分析纯)
b.氢氧化钠(分析纯)预先配成10%溶液
c.盐酸(分析纯)预先配成5%溶液
d.乙酸(分析纯)
e.次氯酸钠溶液(化学纯)
f.淀粉液1%
g.硫代硫酸钠标准液1/2Na2S2O3的浓度0.01ml/L
A3 测试准备工作
A3.1 试验条件
试验氯水浓度 C=5.0±0.5mg/L
水的流速 u=36m/h(1cm/s)
装炭高度 L=1.0±0.1cm
A3.2 测试装置(见图A1)
A3.3 试验用氯水的制备
A3.3.1 分析次氯酸溶液原始浓度
A3.3.1.1 量取次氯酸钠溶液2mL于200mL容量瓶中,用蒸馏水稀释至刻线。
A3.3.1.2 将上述稀释液倾入500mL三角瓶中,加碘化钾约0.5g,再加10mL乙酸。
A3.3.1.3 用硫代硫酸钠标准溶液滴定至淡黄色,加入淀粉液约1mL并继续滴定至蓝色消失为止。
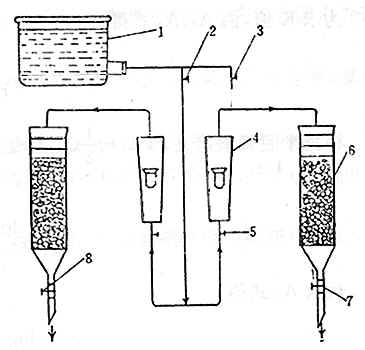
图A 半脱氯值试验装置图
图中:1——水槽;2、3、7、8——活塞(或夹子);4——转子流量计;5——调节阀门;6——测定管
A3.3.1.4 按A7式计算次氯酸钠溶液浓度。
C=N1u1×35.45×1000/2 ×mg/L (A7)
式中 N1——硫代硫酸钠溶液1/2Na2S2O3的浓度,mol/L;
u1——硫代硫酸钠溶液滴定毫升数,mL;
C——次氯酸钠溶液浓度,mg/L;
35.45——氯(C1或C1-)的摩尔质量,g/mol。
A3.3.2 配制氯水
A3.3.2.1 在水槽中加入足够(15L以上)蒸馏水,水温保持在20±3°C,再按氯水浓度要求加入适当的次氯酸钠溶液,并用盐酸和氢氧化钠溶液调节其pH值至7.0~7.5。
A3.3.2.2 取200mL氯水按A3.3.1.2和A3.3.1.3所述步骤进行滴定,并按A8式计算其浓度。氯水浓度必须调节到5.0±0.5mg/L 。
C=N1u1×35.45×1000/2 ×mg/L (A8)
式中 C——所配氯水浓度,mg/L;
N1、u1等,意义同A7式。
A3.4 炭样准备
将炭样在研钵中破碎,用试验筛手工筛取1.0~2.5mm筛份约100mL,置于250mL烧杯中,加蒸馏水至炭面以上1cm,煮沸10~15min,冷却后去掉炭粉备用。
对于颗粒尺寸小于2.5mm的炭样,不需破碎及筛选即可直接摄取,经处后备用。
A3.5 转子流量计和测定管校正
A3.5.1 分别求出转子在不同高度时的流量,绘出转子高度与流量关系曲线。
A3.5.2 按GB 7702附录A规定的方法测出测定管的内径。
A3.5.3 计算出流量为36m/h(1cm/s)时转子的高度,并标示在流量计上。
A4 测定步骤
A4.1 装炭样,将测定管下端7关严(或夹紧),先注入适量的蒸馏水(以装好炭样后水面高出炭面2~3mm为宜)管内得有气泡。然后竖直于振荡器上。边振荡边分批加入准备好的炭样,装炭高度为10±0.1cm。炭层装紧密(振荡中炭层颗粒排列的整齐,高度不再变化)后才可停止振荡,炭层内不得有气泡,否则应重新装炭。
A4.2 将装好炭样的测定管按图接好,检查活塞2和调节阀门5是否关严。
A4.3 开启7(这时不应有水流出),再开启2,然后同时打开两个调节阀门5和开启秒表记时,迅速调节好流量。
A4.4 试验开始30min后,用容量瓶分别收集500mL流出液(28min时收集流出液预先洗涤容量瓶),按3.3.1.2和3.3.1.3所述步骤进行滴定,并按A9式计算出水浓度C,同时从水槽中取样200mL测定进水浓度C0。
C=N1u1×35.45×1000/500 ×mg/L (A9)
(方法同A3.3.2.2)。
A4.5 根据A6式计算炭样的半脱氯值,每个样品测定两个结果,平行误差不得超过1cm,取其平均值。
A5 注意事项及说明
A5.1 试验氯水浓度必须控制在5.0±0.5mg/L,由于次氯酸易挥发,配制试验氯水时可适当偏上限。
A5.2 试剂的配制标定和使用期限按GB 601。
附录B 净水器用活性炭pH,氯化物、砷、锌、镉、铅测定方法(补充件)
B1 适用范围
本标准为净水器用活性炭的检验方法。
B2 采样方法
每生产批号,生产年月日及其生产单位,任意取两个以上容器,并分别采集能尽量代表整体的必要量的试样,保存在不受外界气体影响的气密性容器中。
B3 检验项目
pH值,氯化物,砷,锌,镉,铅含量。
B4检验方法
B4.1 一般事项
B4.1.1 化学分析中的用水,在本检验方法中为蒸馏水的去离子水,其导电率为2us/cm以下。
B4.1.2 用未干燥试样进行试验,预先将部分未干燥试样按B4.2求出干燥减量。利用该值将未干燥试样量换算为试样干燥重量。
B4.1.3 一般检验用溶液,按下述方法制备水萃取液和酸萃取液。
B4.1.3.1 水萃取液,准确称取5g试样(换算至干燥重量),将准确量取的500mL去郭子水放入1000mL带塞三角瓶中。用磁搅拌器搅拌30min,用5号滤纸(直径11cm)过滤,弃去初滤液30mL,其余滤液为水萃取液。
B4.1.3.2 酸萃取液,准确称取5g试样(换算至干燥重),预先将10N硝酸加入精制水中,调整pH值为4~5,准确量取500mL溶液,倾入1000mL烧杯中,放入称好的试样,保持微沸10min,冷却后加水至加热前量,用干燥的5号滤纸(直径11cm)过滤,弃去初滤液30mL,余下的用作测定。
B4.2 干燥减量
本方法为测定试样在110~120°C下干燥2h的减量。
B4.2.1 仪器:扁形称量瓶40mm。
B4.2.2 检验操作
称取2g试样于已知重量的扁形称量瓶底部,其厚度尽可能均匀,取下瓶盖将称量瓶和盖子在110~120°C干燥箱中干燥2h,然后置于干燥器中冷却,求出减量g数(a),按B1式计算干燥减量%。
干燥减量=a(g)/试样(g)×100% (B1)
B4.3 pH值
本法为测定试样水萃取液pH值。
B4.3.1 仪器
pHs-3 酸度计
B4.3.2 检验溶液:采用B4.1.3中水萃取液。
B4.3.3 检验操作:将试验溶液在20°C条件下用酸度计测定。
B4.4 氯化物
本法所采取的试样水萃取液是以铬酸钾溶液作指示剂,用硝酸银溶液滴定,求出氯化物含量。
B4.4.1 试剂
(1)铬酸钾溶液:将5g铬酸钾溶于少量去离子水中,加5%硝酸银溶液至生成少量红色沉淀物,然后过滤,其滤液加去离子水100mL。
(2)0.1mol/L氯化钠溶液:预先在500~600°C干燥40~50min,在硫酸干燥器中冷却。称取5.844g氯化钠于1000mL容量瓶中加去离子水至刻度。
(3)0.01mol/L氯化钠溶液:量取100mL0.1mol/L氯化钠溶液于1000mL容量瓶中。加去离子去至刻度。
(4)0.01mol/L硝酸银溶液:称取1.7g硝酸银于1000mL棕色容量瓶中加去离子水至刻度。
标定系数:吸取25mL0.01mol/L氯化钠溶液于三角瓶中,加0.2mL铬酸钾溶液,用0.01mol/L硝酸银溶液滴定至出现淡黄棕色不再消失,求出所需的0.01mol/L硝酸银溶液mL数(a),按B2式计算标定系数:
标定系数-(F)=25/a (B2)
式中 F——0.01mol/L硝酸银溶液标定系数。
本溶液1mL相当于0.355mg氯化物。
B4.4.2 仪器:三角瓶。
B4.4.3 检验溶液,采用B4.1.3试样水萃取液。
B4.4.4 检验操作
吸取50mL检验溶液于三角瓶中,pH值后(1),加0.2mL铬酸钾溶液,用玻璃棒边搅拌边加数滴0.01mol/L硝酸银溶液至出现淡黄褐色(2)。求出所需0.01mol/L硝酸银溶液mL数(a),按B3式计算氯化物%:
氯化物%=aF×0.355×0.01/试样(g)×50/500×100 (B3)
式中 F——0.01mol/L硝酸银溶液标定系数。
注:(1)检验溶液为酸性时用0.02mol/L氢氧化钠中和,碱性时用2.02mol/L硫酸中和。
(2)反应终点时,在另一同型三角瓶中取50mL去离子水,最好与这时所加的0.2mL铬酸钾溶液的颜色进行比较来判断。
B4.5 砷含量的测定
本法将试样酸萃取液中的砷制成砷化氢,用二乙氨基二硫代甲酸银吡啶溶液吸收时呈橙黄色—红色,与同法处理得到的标准液的颜色相比较,求出砷含量。
B4.5.1 试剂
(1)氯化亚锡溶液;称取40g氯化亚锡(2个结晶水,不含砷)溶于100mL盐酸中,该溶液在使用前配制。
(2)碘化钾溶液:称取15g碘化钾溶于100mL去离子水中,该溶液在使用前配制。
(3)不含砷锌粒。
(4)砷标准液
预先将三氧化二砷(标准试剂)在乳钵中研细,在105~110°C恒温干燥箱中干燥3~4h,置于硫酸干燥器中,冷却后从中称取0.132g于500mL烧杯中,加5mL5mol/L氢化钠溶液溶解,加400mL精制水,而后再加1mol/L硫酸进行中和(用石蕊试纸鉴定)后称入1000mL容量瓶中,用少量去离子水冲洗烧杯,将冲洗液并入容量瓶中加去离子水至刻度,制成砷贮存液。
吸取砷贮存液10mL于另一个1000mL容量瓶中,加10mL1mol/L硫酸后加去离子水至刻度。
1mL砷溶液含砷(As)1.0µg。
(5)乙酸铅溶液:称取10g已酸铅(3个结晶水)加100mL去离子水和1滴6mol/L乙酸溶解,密闭保存。
(6)吸收溶液1称取0.25g二乙氨基二硫代甲酸银(C5H10NS2、Ag)研碎后用少量氯仿溶解,加入1.0mL三乙酸胺(C6H15NO3),再用氯仿稀释到100mL,必要时,静置后过滤至棕色瓶内,贮存于冰箱中。
B4.5.2 仪器
(1)砷检验装置:由三角发生瓶、导管和吸收管组成。
(2)光度计:分光光度计。
(3)检验溶液:采用B4.1.3试样酸萃取液。
(4)检验操作
吸取100mL检验溶液于瓷表面皿上,在水浴上蒸发浓缩到25mL,移入砷检验装置发生瓶中,将蒸发皿用少量水冲洗,并将洗液并入发生瓶中,加5mL盐酸,并加去离子水至40mL左右。再加2mL磺化钾溶液静置2~3min后加1mL氯化亚锡溶液混匀静置15min左右。往发生瓶内加3g锌粒,立即将发生瓶、有乙酸铅棉花的导管和加入5mL二乙氨基二硫代甲酸银溶液的吸收管连接起来。在常温下产生氢氯1h,以吸收管中的溶液制成检测液。
在几个砷检验装置发生瓶中分别吸取适量的(1~20mL)砷标准液,分别加入5mL盐酸,加水至40mL,另外将5mL盐酸加到另一砷检验装置发生瓶中,加水40mL左右,以下分别与检验溶液进行同样处理,将其制成标准液和空白试验液。
将检验溶液、标准液和空白试验液吸入比色管中,用分光光度计测定在波长540mm附近的吸光度,根据测得的检验溶液的吸光度在砷含量标准曲线上求出检验溶液中砷含量µg数(a),按B4式算出砷的µg/g值。
砷(As µg/g)=a/试样(g)×100/500 (B4)
B4.6 锌含量的测定
B4.6.1 吸光光度法,本法用试样酸萃取液、在弱酸性中存在硫代硫钠的情况下,用双硫腙四氯化碳萃取锌时,呈紫色,与同样处理得到的标准液颜色相比较,求出锌含量。
B4.6.1.1 试剂
(1)锌标准溶液:称取0.4398g(ZnSO4·7H2O)溶于去离子水中,加入10mL浓HCI,用去离子水在1000mL容量瓶中稀至刻度,摇匀,使用前取此溶液10.00mL,用去离子水在1000mL容量瓶中稀至刻度,摇匀。
此液1.0mL含1.00µg锌。
(2)0.1%双硫腙四氯化碳贮备溶液:称取0.10g双硫腙(C13H12N4S),在干燥的烧杯中用四氯化碳溶解后稀释至100mL,倒入棕色瓶中,此溶液置冰箱内保存,可稳定数周。
如双硫腙不纯,可用下述方法纯化:称取0.20g双硫腙,溶于100mL氯仿,经脱脂棉过滤于250mL分液漏斗中,每次用20mL3+97稀氨水连续反萃取数次,直至氯仿相几乎无绿色为止,合并水相至另一分液漏斗。每次用四氯化碳10mL振荡洗涤水相两次,弃去四氯化碳相。水相用1+9硫酸溶液酸化至有双硫腙析出,再每次用100mL四氯化碳萃取两次,合并四氯化碳相,倒入棕色瓶中。置冰箱内保存。
(3)双硫腙四氯化碳溶液,临用前,吸取适量双硫腙四氯化碳腙贮备溶液(2),用四氯化碳稀约30倍,至吸光度为0.4(波长535nm,1cm比色皿)。
(4)乙酸—乙酸钠缓冲溶液(pH4.7),称取68g乙酸钠(NaC2H3O2、3H2O),用去离子水溶解后稀释至250mL,另量取冰乙酸31mL,用纯水稀释至250mL,将上述两种溶液等体积混合。
如试剂不纯,将上述混合液置于分液漏斗中,每次用10mL双硫腙四氯化碳溶液(3)萃取,直至四氯化碳相呈绿色为止,弃去四氯化碳相;向水相中加入10mL四氯化碳,振摇洗涤水相,弃去四氯化碳相。如此反复数次,至四氯化碳相不显绿色为止,用滤纸过滤水相于试剂瓶内。
(5)25%硫代硫酸钠溶液,称取25g硫代硫酸钠(Na2S2O3、5H2O),溶于100mL去离子水中,如试剂不纯,按(4)所述方法纯化。
(6)0.1%甲基红指示剂,称取0.1g甲基红(C15H15N3O2),用60mL95%乙醇溶解后,加纯水至100mL。
(7)1+1氨水溶液。
(8)1+7乙酸溶液,将10mL冰乙酸溶于70mL去离子水中。
(9)四氯化碳。
B4.6.1.2 仪器
所用玻璃仪器均需用1+1硝酸洗涤,然后再用不含锌的去离子水冲洗干净,不得用自来水冲洗。
(1)60mL分液漏斗。
(2)10mL比色管。
(3)分光光度计。
B4.6.1.3 检验溶液,用B4.1.3试样酸萃取液。
B4.6.1.4 检验操作
吸取2.00mL检验溶液于60mL分液漏斗中,另取分液漏斗8个,依次加入锌标准液1.0~8.0mL,向水样与标准中各加去离子水至10mL,各滴甲基红指示剂,用1+1氨水调节液刚显黄色,再滴加乙酸溶液至红色(pH约4.4),加5mL四氯碳,振荡萃取甲基红,弃去有机相,向各分液漏斗中加入5.0缓冲溶液混匀,再加入1.0mL硫代硫酸钠溶液,混匀,再加入10.0mL双硫腙四氯化碳溶液,强烈振荡4min,静置分层。
用脱指棉或卷细的滤纸擦去分液漏斗颈内的水,弃去最初2~3mL有机相,收集其后的有机相于干燥的10mL比色管内。
于535nm波长下,用1cm比色皿,以四氯化碳为参比,测定样品标准液列溶液的吸光度。
绘制标准曲线,在曲线上求出锌的µg量(a),按B5式计算锌的µg/g含量:
锌(Zn µg/g)=a/试样×2/500 (B5)
B4.6.2 原子吸光光度法
本法将试样酸萃取液稀释,直接用原子吸光光度法求出锌含量。
B4.6.2.1 试剂
锌标准液:采用B4.6.1中的试剂。
B4.6.2.2 仪器
玻璃仪器:与B4.6.1中的相同。
原子吸收分光光度计。
B4.6.2.3 检验溶液:采用B4.1.3试样酸萃取液。
B4.6.2.4 检验操作
吸取10mL检验溶液于100mL容量瓶中,加去离子水至刻度,作为检验溶液。
取适量的锌标准液(1~10mL)于数个100mL容量瓶中,每只加10mL1M硝酸,再加去离子水至刻度,于另一100mL容量瓶中加入10mL 1M硝酸,加去离子水至刻度。
将检验溶液、标准液和空白试验液用原子吸光光度计,使用锌中空阴极管在波长213.8nm测定吸光度,根据所得到的检验溶液吸光度在锌含量标准曲线上,求出检验溶液中锌的µg含量(a),按B6式计算锌的µg/g含量。
锌(Zn µg/g)=a/试样(g)×10/500 (B6)
B4.7 镉含量的测定
B4.7.1 吸光光度法:本法用试样酸萃取液,在碱性氰化钾存在下,用双硫腙三氯甲烷溶液萃取镉,再用酒石酸溶液进行逆萃取,在碱性氰化钾中,用双硫腙三氯甲烷溶液再萃取时,呈淡红色。与同样处理到的标准液颜色相比较,求出镉含量。
B4.7.1.1 试剂
(1)柠檬酸铵溶液,称取40g柠檬酸铵溶解于去离子水中,并加去离子水至100mL刻度。
(2)酒石酸钾钠溶液:称取250g酒石酸钾钠加去离子水溶解至1000mL刻度。
(3)氢氧化钠、氰化钾溶液(A):称取400g氢氧化钠和10g氰化钾溶于去离子水中,直至1000mL刻度。置于聚乙烯瓶中贮存。本溶液保存期为1~2个月。
(4)氢氧化钠、氰化钾溶液(B):称取400g氢氧化钠和0.5g氰化钾在去离子水中溶解,并加水至1000mL刻度。置于聚乙烯瓶中贮存。本溶液保存期为1~2个月。
(5)盐酸羟胺溶液:称取20g盐酸羟胺加去离子水溶液,并加水至100mL刻度。
(6)精制三氯甲烷:加5%三氯甲烷容量的硫酸振荡混匀,反复操作至硫酸层为无色。其次,再用20%(容量)的1mol/L氢氧化钠溶液洗涤两次,再用去离子水洗,然后加氧化钙进行蒸馏。加入20%(容量)馏出液的0.5%盐酸羟胺溶液振荡混匀,待分层后,将三氯甲烷层用干燥的滤纸过滤。然后加1%(容量)的乙醇(分析纯)置于棕色瓶中,放于冷暗处保存。
(7)浓双硫腙三氯甲烷溶液:将双硫腙在研钵中研成细粉,取100mg双硫腙加1000mL精制三氯甲烷溶解,放于冷暗处保存。
(8)稀双硫腙三氯甲烷溶液:取浓双硫腙三氯甲烷溶液100mL,加精制三氯甲烷稀释至1000mL刻度,置于棕色瓶中,放于冷处保存,在使用期间加温至室温。
(9)酒石酸溶液:称取20g酒石酸在去离子水中溶解,并加至1000mL刻度,放于冷暗处保存。
(10)镉标准液:称取0.100g金属镉于烧杯中,加20mL去离子水和5mL盐酸,并加2~3滴硝酸,在水浴上加热溶解,并蒸发至干固。冷却后加10mL盐酸溶解移入1000mL容量瓶中,烧杯用去离子水洗净,并将洗液并入容量瓶中,加去离子水1000mL至刻度,制成隔贮存液,置于聚乙烯瓶中贮存。使用时吸取镉贮存液10mL于1000mL容量瓶中,加10mL盐酸,再加去离子水至1000mL刻度。
1mL该溶液含镉10µg。
B4.7.1.2 仪器
光度计:分光光度计。
玻璃仪器:与B4.6.2相同。
B4.7.1.3 检验溶液:用B4.1.3试样酸萃取液。
B4.7.1.4 检验操作
吸取100mL检验溶液于200mL分液漏斗中,加6mL柠檬酸铵溶液混合均匀,加3mL酒石酸钾钠溶液,加15mL氢氧化钠、氰化钾(A)溶液和3mL盐酸羟胺混后,再加15mL双硫腙三氯甲烷振荡1min静置分层。
将分离的三氯甲烷层移入第2号装有25mL酒石酸溶液的100mL分液漏斗中。在第1号分液漏斗中加10mL精制三氯甲烷振荡1min静置分层,将分离的三氯甲烷并入第2号分液漏斗中(1)。
注:(1)该操作应立即进行,第2号分液漏斗中不要加入水层。
将第2号分液漏斗振荡2min后静置分层,将分离的三氯甲烷层舍弃,再加5mL精制三氯甲烷振荡1min,仍将三氯甲烷层舍弃。
在水层中加入0.3mL盐酸羟胺溶液,并准确加入15mL稀双硫腙三氯甲烷溶液和5mL氢氧化钠、氰化钾溶液(B)振荡1min静置,用铺有脱指棉的漏斗过滤三氯甲烷,置于干燥的试管中,制成检验溶液。
取适量的镉标准液(1~6mL)于200mL分液漏斗中,分别加去离子水100mL左右,在另一200mL分液漏斗中,加100mL去离子水,以下与检验溶液进行同样处理所得到的三氯甲烷层,作为标准液和空白试验液。
将检验溶液、标准液和空白试验液移入比色皿中,用分光光度计测定波长518nm附近的吸光度,根据所得至的检验溶液的吸光度,在镉含量标准曲线上,求出镉µg含量(a),按B7式计算镉的µg/g含量。
镉(Ca µg/g)=a/试样(g)×100/500 (B7)
B4.7.2 原子吸收分光光度法
本法将试样酸萃取液蒸发浓缩,直接利用原子吸收分光光度法,求出镉含量。
B4.7.2.1 试剂
镉标准液,与B4.7.1.1(10)相同。
B4.7.2.2 仪器
原子吸收分光光度计。
玻璃仪器与B4.6.1相同。
B4.7.2.3 检验溶液,采用B4.1.3试样酸萃取液。
B4.7.2.4 检验操作
准确吸取200mL检验溶液于瓷表面皿上,在水浴上蒸发浓缩至10mL,冷却后加去离子水至总量为20mL,制成检验溶液。
取适量镉标准液(2~10mL),分别加入几个100mL容量瓶中,每瓶各加10mL1mol/L硝酸,加精制水至100mL刻度。另外,在100mL容量瓶中,取10mL1mol/L硝酸溶液,加去离子水至100mL刻度,制成标准液和空白试验液。
将检验溶液、标准液和空白试验液分别在原子吸收分光光度计上,用镉中空阴极管测定波长228.8nm处的吸光度,根据检验溶液的吸光度在镉含量标准曲线上,求出镉µg含量(a),按B6式计算镉的µg/g含量:
镉(Cd µg/g)=a/试样(g)×200/500 (B6)
B4.8 铅含量的测定
B4.8.1 吸光光度法
试样酸萃取液,在柠檬酸铵、盐酸羟胺和氰化钾存在下,用双硫腙四氯化碳萃取铅,再稀硝酸处理,再次从水中逆萃取四氯化碳层,在逆萃取液中加入氨性氰化钾—柠檬酸溶液,用双硫腙四氯化碳进一步萃取时所呈现的鲜红色与同法处理所得到的标准液颜色相比较,求出铅含量。
B4.8.1.1 试剂
(1)柠檬酸铵溶液:称取50g柠檬酸铵,加100mL去离子水溶解,滴加10mol/L氨水使pH为8.5~9.0,调整pH时为放热反应,因而在容器外部用水冷却。
将上述配制的溶液移入200mL分液漏斗中,为除去含有不纯物的重金属,加入10mL双硫腙四氯化碳贮存液振荡混匀,静置分层,并将四氯化碳层舍弃,反复操作至双硫腙四氯化碳溶液保持原有的绿色为止。然后为除去过量的双硫腙,加10mL精制四氯化碳振荡混匀,反复进行这样的操作至四氯化碳无色为止。
(2)盐酸羟胺液:称取20g盐酸羟胺于烧杯中,加65mL去离子水溶解。滴加10mol/L氨水,在pH计上调整溶液pH为8.5~9.0。调整pH时为放热反应,因而在容器外部用冰冷却。
(3)氰化钾溶液:称取20g氰化钾在去离子水中溶解,溶解后加去离水至200mL刻度。由于氰化钾溶液不能进行精制,为调配其纯度,吸取5mL氰化溶液于50mL带塞比色管中,加5mL双硫腙四氯化碳溶液振荡混匀。如果双硫腙四氯化碳层不呈现紫红色即可使用,当呈现紫红色时,则须用纯的氰化钾。
(4)氨性氰化钾:柠檬酸溶液:在500mL氨水中加入10g氰化钾、10g柠檬酸使之溶解,加去离子水至1000mL刻度。
由于该溶液不能进行精制,可用一部分溶液进行与氰化钾溶液一样的试验。
(5)百里香酚蓝指示剂:在研体中研细称取0.1g百里香酚蓝,加10.8mL0.01mol/L氢氧化钠溶液,研磨至全部溶解后,移入250mL容量瓶中,加去离子水至250mL刻度。
(6)精制四氯化碳。
(7)双硫腙四氯化碳贮存液:采用B4.6.1试剂。
(8)双硫腙四氯化碳溶液:采用B4.6.1试剂。
(9)铅标准液称取0.2g硝酸铅于1000mL容量瓶中,再加1mL硝酸于100mL去离子水中溶解,再加去离子水至1000mL刻度,作为铅贮存液。使用时吸取该溶液10mL于200mL容量瓶中,加去离子水至刻200mL刻度。再从该溶液中吸取10mL于250mL容量瓶中加去离子水至刻度。
1.0mL该溶液含铅0.25µg。
B4.8.1.2 仪器
光度计:分光光度计。
玻璃仪器:与B3.6.1相同。
B4.8.1.3 检验溶液:采用B4.1.3试样酸萃取液。
B4.8.1.4 检验操作
吸取50mL检验溶液于100mL第1号分液漏斗中,再加10mL柠檬酸铵液和数滴百里香酚蓝指示剂,直至溶液呈淡暗绿色为止,再滴加氨水(pH为8.5~9.0)。然后,在溶液中加2mL盐酸羟胺溶液和4mL氰化钾溶液,混合后再加5mL双硫腙四氯化碳溶液,振荡30s,静置分层,将四氯化碳层移入100mL第2号分液漏斗中。在第1号分液漏斗中再加5mL双硫腙四氯化碳溶液,振荡30s静置分层,将四氯化碳层并入第2号分液漏斗中。在第2号分液漏斗中加20mL0.1mol/L硝酸,激烈振荡1min静置分层,将分离的四氯化碳层舍弃。水层加去离子水50mL左右,然后加4mL氨性氰化钾、柠檬酸溶液,再加5mL双硫腙四氯化碳溶液,振荡1min后,静置分层。将四氯化碳层移入试管,将此作为检验溶液。
吸取适量的铅标准液(1~20mL),分别放入数个100mL分液漏斗中,各加去离子水至总量为50mL。再取50mL去离子水放入另外100mL的分液漏斗中。分别与检验溶液进行同样处理,在试管中取所得的四氯化碳层,将它作为标准液和空白试验液。在比色皿中放入检验溶液、标准液和空白试验液,用分光光度计测定波长510nm附近的吸光度,根据所得检验液的吸光度,在铅含量标准曲线上,求出检验溶液的铅µg量(a),按B9式计算铅µg/g含量:
铅(Pb µg/g)=a/试样(g)×50/500 (B9)
B4.8.2 原子吸收分光光度法
本法将试样酸萃取液蒸发浓缩,直接用原子吸光光度法,求出铅含量。
(1)试剂
铅标准液:在500mL容量瓶中加入300mL1mol/L硝酸,然后准确加入5mL铅贮存液(B4.8.1试剂),再加1mol/L硝酸至500mL刻度,制成铅标准液。
1mL该溶液含铅1.25µg
(2)仪器
原子吸收光光度计。
玻璃仪器:与B4.6.1相同。
(3)检验溶液:采用B4.1.3试样酸萃取液。
(4)检验操作:检验溶液按B4.7.2操作。
分别吸取适量的铅标准液(2~50mL)放入数个100mL容量瓶中,各加10mL1mol/L硝酸,加去离子水至100mL刻度,另在100mL容量瓶中取10mL1mol/L硝酸加去离子水至100mL刻度。这些分别作为标准液和空白试验液。
将检验溶液、标准液和空白试验液在原子吸收分光光度计上用铅中空阴极管测定波长283.3nm的吸光度,根据得到的检验溶液的吸光度,在铅含量标准曲线上,求出检验溶液的铅µg含量(a),按B10式计算铅ppm含量:
铅(µg/g)=a/试样(g)×200/500 (B10)
附录C 总溶解性有机碳检验方法(补充件)
水中溶解着许多不同有机物。在这些碳化合物中有些可以经生物或化学的过程进一步氧化,这些部分可以通过生化需氧量(BOD)及化学需氧量(COD)予以测定。但是,水中还存在着既不为BOD也不为COD测出的有机碳。总溶解性有机碳DOC的检验法则是可以测定水中所有溶解性有机碳的合适方法。本检验法采用燃烧—红外法。
C1 应用范围
C1.1 本法适用于测定生活饮用水中溶解性有机碳。
C1.2 本法最低检测量为1mg/L。
C1.3 采集水样,贮在玻璃瓶中,送化验室立即测定,如不能即时测定,可将其保存在温度为4°C的环境中,尽量不暴露在光和空气中并尽量减少贮存时间。
C2 原理
将微量水样在净化的空气流中注射至已加热的填弃管中,水样气化,有机碳被氧化为CO2及H2O0用红外分析器测量CO2,测定总碳和无机碳,用差减法计算总有机碳。
C3 试剂
C3.1 重蒸馏水:用无CO2重蒸馏水配制空白和标准溶液。
C3.2 DOC标准溶液:称0.850g烘干的邻苯二甲酸氢钾(C6H5KO4)溶于CO2的重蒸馏水中,稀释至1000mL,1mL=0.4mg碳。
C3.3 标准无机碳溶液:称1.40g碳酸氢钠和1.73g(于500~600°C烘干30min,取出在干燥皿中冷却至室温)碳酸钠,稀至1000mL,1mL=0.4mg。
C4 仪器
总有机碳分析仪。
C5 测定步骤
C5.1 按照仪器操作要求,使仪器达到正常工作状态。
C5.2 标准曲线制备。
C5.2.1 在DOC标准溶液中准确吸取0、5.0、10.0、15.0、20.0、25.0mL于100mL容量瓶中,稀释成0、20.0、40.0、60.0、80.0、100.0mg/L的标准溶液系列。
C5.2.2 用微量注射器吸取20µL标准溶液,注射进样,每只样品重复三次,使峰高误差不超过1刻度,取平均值。记录标准及1份稀释水空白的峰高。
C5.2.3 在无机碳标准溶液中准确吸取0、5.0、10.0、15.0、20.0、25.0mL于100mL容量瓶中,稀释配制成0、20.0、40.0、60.0、80.0、100.0mL/L标准系列。
C5.2.4 用微量注射器吸取20µL标准溶液,注射进样,每只样品重复三次,使峰高误差不超过一刻度,取平均值,记录标准及一份稀释水空白的峰高。
C5.3 样品注射
C5.3.1 水样预处理 水样在离心管中经2000n/min离心机离心10min。
C5.3.2 用微量注射器吸取预处理后的水样20µL注射进样,每只水样重复三次,使峰高误差不超过一刻度,取平均值。
C5.4 计算
C5.4.1 从标准峰高减去空白值,按标准浓度与峰高制成的总碳与无机碳的回归方程。
C总=a1h+K1 (C1)
C无=a2h+K2 (C2)
式中 C总——总碳浓度,mg/L;
h——峰高;
C无——无机碳浓度,mg/L;
K1和K2——常数;
a1和a2——常数。
C5.4.2 按C1(式)和C2(式)计算的总碳和无机碳两者之差为总溶解性有机碳。
DOC=C总-C无 mg/L (C3)
C5.4.3 精密度
本法精密度为1~2%。
附录D 水样Ames致突变试验方法(补充件)
D1 定义
Ames试验系列用微生物的营养缺陷型突变株的回复突变性能来检测环境致突变物,有些致突变物需经哺乳动物细胞代谢活化后,才通体现其致突变作用,Ames等人研究并提出了鼠伤寒沙门氏菌/哺乳动物肝微粒体试验法,它是在动物体外将待测物质经肝微粒体酶系活化后,检查其所诱发的沙门氏菌回变菌落数,即由不能自行合成组氨酸的营养缺陷型突变株(his-)回复为能自行合成组氨酸的(his+)菌落数。
D2 材料和试剂
D2.1 材料
D2.1.1 菌株 常用于水致突变试验的鼠伤寒沙门氏菌采用两种(Salmonella typhimurinm)组氨酸缺陷型菌株,即TA98,TA100,其中TA98用以检出可引起移码突变的致突变物,TA100用以检出可引起碱基对置换突变的致突变物,凡用作试验的菌株,均需经五项主要性状的鉴定,通过后方可使用。
D2.1.2 XAD-2树脂 将市售XAD-2树脂在索氏抽提器中,用乙醚、丙酮、甲醇溶液分别回流8h,然后保存在甲醇液中备用。
D2.1.3 水样浓缩 取水样40L(混浊水须经过滤)以25~30mL/min的流量通过装有10g洗净的XAD-2树脂的层析柱,滤毕用30mL丙酮,或30mL30%丙酮-甲醇混合液,以滤水时的同样流量将吸附于树脂上的有机物洗脱,洗脱液于45°C水浴上挥干,然后用二甲亚砜(DMSO)溶解定容至4mL,再倍比稀释成每0.1mL含0.25L、0.5L、1.0L、水样的三个浓度组备用。
D2.2 阳性致突变物
D2.2.1 甲基甲烷磺酸酯(MMS)、浓度0.2mL/mLDMSO溶液,于4°C冰箱保存,不稳定。
D2.2.2 2.7-二氨基芴(2.7AF)浓度20mg/mLDMSO溶液,于4°C冰箱保存,尚稳定。
D2.2.3 2-氨基芴(2AF)浓度2mg/mLDMSO溶液于4°C冰箱保存。
D2.3 肝微粒体酶(S-9上清液 )
D2.3.1 诱导 选成年雄性大鼠3只(每只体重约200g左右)按500mg/kg一次腹腔注射Aroclor1254(或国产多氯联苯)注射液用玉米油配制浓度为200mg/mL,注射后第5天杀鼠,杀鼠前12h禁食(可饮水)。
D2.3.2 制备肝匀浆,大鼠断头处死,以无菌操作,打开腹腔,用冷冻的0.15MKC1溶液门脉灌注,摘出肝脏,称重,用冷冻0.15MKC1溶液洗涤3次,以每克肝加3倍冷冻0.15MKC1溶液,放入组织捣碎机,20000n/min 1min,制成匀浆,将肝匀浆于低温高速离心机9000g(11000n/minRPR-16)离心10min(0~4°C)取上清液为S-9组分,用小安瓿分装,每瓶2mL,封口,以干冰丙酮冻结后,于液氮或-80°C低温冷箱保存,备用,用时在室温下解冻,剩余部分应丢弃,每批S-9应作活性检验。
D2.3.3 配制S-9混合液,每1mL S-9混合液中,含有表D1内容物。
表D1 S-9混合液的配制 | S-9上清液 | 0.1mL | | 0.4M MgCI2 | 0.02mL | | 1.65M MCI | 0.02mL | | IM 葡萄糖-61-磷酸 | 0.005mL | | 0.1M 辅酶 Ⅱ(NADP) | 0.04mL | | 0.2M磷酸盐缓冲液(pH7.4) | 0.50mL | | 灭菌蒸馏水 | 补足总量为1mL | 可先将上述各溶液配制好,除菌后,放冰箱备用,上述各项操作中所用器皿、刀剪,溶液均需保持无菌,并在0~4°C下操作。
D2.4 培养基
D2.4.1 营养肉汤、牛肉膏0.5%,蛋白胨1%,氯化钠0.5%调pH至7.2。分装中试管,每管5mL,高压灭菌备用。
D2.4.2 营养琼脂,在D2.4.1营养肉汤中加琼脂2%即成,按需分装,灭菌备用。
D2.4.3 底层(基本养基)(即最低营养培养基)
D2.4.3.1 Vogel-Bonner(V-B)低限培养基E(50×)见表D2。
表D2 Vogel-Bonner(V-B)低限培养基E(50×)的配制 | 成 分 | 每 升 | | 温蒸馏水(45°C) | 670mL | | 硫酸镁(MgSO4·7H2O) | 10g | | 柠檬酸 | 100g | | 磷酸氢二钾(K2HPO4)无水 | 500g | | 磷酸氢铵钠(NaHNH4PO44H2O) | 175g | 用一只2L烧杯,用温水加(热)温,使每种盐完全溶解后,再加入下一种盐,调整容量至1L,然后120°C20min灭菌,冷却至室温4°C冰箱保存。
D2.4.3.2 40%葡萄糖溶液 葡萄糖40g,加蒸馏水100mL112°C,10min灭菌。冷却至室外温,4°C冰箱保存。
D2.4.3.3 琼脂15g,加蒸馏水930mL,120°C20min灭菌。
D2.4.3.4 将D2..3.1、D2.4.3.2、D2.4.3.3、趁热混合,降温到55°C左右时倒入无菌平皿(直径9cm)每平皿250mL左右,此琼脂平板可置室温保存。
D2.4.4 表层培养基,琼脂0.6%,氯化钠0.5%,按所配表层培养基总量加入1/10体积的0.5m Mol L—组氨酸及0.5mMol生物素混合均匀后,趁热分装小试管,每管2mL,灭菌备用。
D3 致突变试验方法
D3.1 试验用菌液的准备 用无菌小木勺刮取TA98及TA100冻干菌种少许分别接种入5mL营养肉汤试管内。37°C水浴振荡培养9~12h,活菌数在1~3×109/mL范围供诱变试验用,此菌液可在4°C冰箱内保存,供用一周,但不宜转管接种。
D3.2 致突变试验操作步骤 先在平皿盖上做好标记,取融化了并保温45°C的表层培养基一管(2nL),依次加入菌液0.1mL(需活化的加S-9混合液0.5mL),充分混合后迅速倒在底层培养基上(全部操作不要超过20s),平铺待凝,注意避光,37°C培养48h,观察结果,每一水样浓度需平行接种三个平皿。
D3.3 对照 每次试验均设置自发回变(即在表层培养基中不加待测物)及已知致突变物(TA100菌株加S-9混合液的用2AF浓度为20µg/10µL,不加S-9的用MMS浓度为2µL/10µL,TA98菌株加S-9用2AF,浓度为20µg/10µL,不加S-9的用2.7AF浓度为200µg/10µL)作为对照,以检验所用方法及步骤之可靠性,对照试验亦需平行接种三只平皿。
D4 结果与评价
D4.1 结果 计数每一浓度三个平皿培养基上的回变菌落数的平均数,凡诱发回变的his+菌落数为自发回交his+菌落数的2倍以上时,并有剂量反应关系,即为致突变物,可以用突变率表示之。见式D1。
突变率=诱发回变his+菌落数/自发回变his+菌落数 (D1)
只有当突变率大于等于2.0时才为阳性,当待测物浓度达到1L水样浓缩物/皿(1)时仍为阴性者,可报告为阴性结果。
注:(1)在一般试验中当水样浓缩物浓度达到1L/皿时不出现阳性反应,就定为该水样致突变试实验为阴性结果,但也可根据不同要求对水样浓缩物浓度进行增减。
在观察结果时,于平皿上his+回变菌落下必须有一层菌苔,作为背衬方可确认为his+回变菌落,该菌苔系his-菌利用表层培养基中所含之微量组氨酸生长分裂数次所形成,这种生长对产生诱变作用是必要的。
D5 菌株性状鉴定
D5.1 试剂
D5.1.1 组氨酸/生物素培养基
无菌操作,组氨酸/生物素培养基的配制见表D3。
表D3 组氨酸/生物素培养基的配制 | 成 份 | 每 升 | | 琼 脂 | 15g | | 蒸馏水 | 914mL | | 50×VB盐溶液 | 20mL | | 40%葡萄糖 | 50mL | | 灭菌盐酸组氨酸水溶液(每400mL 水含2g) | 10mL | | 灭菌0.5mM生物素 | 6mL | 分别高压,将灭菌40%葡萄糖,v-B盐和组氨酸加进热的琼脂溶液中,混匀,倒平板。
D5.1.2 氨苄青霉素培养基
无菌操作,氨苄青霉素培养基的配制见表D4。
表D4 氨苄青霉素培养基 | 成 份 | 每 升 | | 琼 脂 | 15g | | 蒸馏水 | 914mL | | 50×VB盐溶液 | 20mL | | 40%葡萄糖 | 50mL | | 灭菌盐酸组氨酸水溶液(每400mL 水含2g) | 10mL | | 灭菌0.5mM生物素 | 6mL | | 无菌氨苄青霉素溶液(8mg/mL0.02M NaOH) | 3.15mL | 混匀,冷却到大约50°C,再加入无菌生物素和氨苄青霉素溶液,混匀倒板。
D5.1.3 结晶紫溶液
无菌配制,称取100mg结晶紫,溶于100mL灭菌蒸馏水中。
D5.1.4 15W紫外线灯
D5.2 菌株鉴定
几株菌可在同一平皿上鉴定。
D5.2.1 组氨酸需要
用无菌棉拭子或金属耳沾取少许各菌株培养液,然后平行划线接种于组氨酸/生物素平皿,37°C培养24h,结果:应生长,在不含组氨酸的平皿上应不生长。
D5.2.2 深度粗糙(rfa)特性
先用灭菌棉拭子或金属耳沾取少许各菌株培养液,平行划线接种于营养琼脂平皿,培养液干后,在平板中线与接种的垂直方向贴放6mm宽浸有结晶紫溶液液的滤纸条,37°C培养24h,结果:滤纸条周围形成透明抑菌带,直径约14mm。
D5.2.3 △uvrB特性 紫外线敏感试验
先用灭菌棉拭子沾取各菌株培养液少许,平行划线接种于营养琼脂平板,然后在垂直距平板33cm处用15W紫外线灯照射8s,照射时平板中线一侧用黑纸板遮盖,37°C培养24h,结果:紫外线照射部分无菌生长。
D5.2.4 R 因子鉴定 抗氨苄青霉素试验
用无菌棉拭子沾取各菌株培养液少许,平行划线接种于氨苄青霉素平板,37°C培养24h,结果:有R因子的在划线处有菌生长;无R因子的,在划线处无菌生长。
D5.2.5 自发回变鉴定
将0.1mL各菌株培养液加入2mL45°C的表层培养液中,充分混匀后倒入低限葡萄糖平板,37°C培养48h,作菌落计数结果,在不加S-9混合液的低限葡萄糖平板上,自发回变数TA98为35~50、TA100 120~200。
TA98、TA100是带有R因子的菌株。
D6 S-9的活性检验
在每制备一批新的S-9组分时,为了确证其代谢活性,必须对其活性进行检验,可以用黄曲霉素B,或2-氨基芴等作阳性对照检验,结果表明应有良好的活性,才能使用。 附加说明:
本标准由建设部标准定额研究所提出。
本标准由建设部水处理设备器材标准技术归口单位中国市政工程华北设计院归口。
本标准由上海市自来水公司,上海市自来水公司给水设备工程公司(原节水设备总厂)负责起草。
本标准主要起草人:岳舜琳、张珍钰、吴国平。
本标准委托上海市自来水公司负责解释。
| 

 (A2)
(A2)






